reakcja chemiczna, przemiana chemiczna,
przemiana jednych substancji, zwanych substratami, w inne substancje, zwane produktami reakcji chemicznej;
reakcja chemiczna
Encyklopedia PWN
substratami i produktami, ogólnie — reagentami, mogą być atomy, cząsteczki, jony lub rodniki. Jeśli wszystkie reagenty występują w tej samej fazie (np. są gazami) reakcję chemiczną nazywa się reakcją homogeniczną, jeśli w różnych fazach — reakcją heterogeniczną. Reakcje homogeniczne zachodzą jednocześnie w całej fazie (całej objętości układu), heterogeniczne — głównie na granicy faz. Stosunki ilościowe między reagentami podaje równanie stechiometryczne, zwane równaniem chemicznym. W równaniu tym substraty umieszcza się po lewej stronie, produkty po prawej: αA + βB = γC + δD, gdzie α, β, γ i δ są współczynnikami stechiometrycznymi; równanie chemiczne odzwierciedla prawo zachowania masy spełnione podczas reakcji chemicznej, podaje jej sumaryczny, a nie rzeczywisty przebieg. Reakcje chemiczne zwykle składają się z kilku następujących po sobie etapów zwanych reakcjami elementarnymi (procesami elementarnymi). Fotochemiczna synteza chlorowodoru przedstawiona równaniem H2 + Cl2 = 2HCl, które interpretuje się: jedna cząsteczka (lub jeden mol) wodoru reaguje z jedną cząsteczką (jednym molem) chloru, dając dwie cząsteczki (dwa mole) chlorowodoru, jest w istocie reakcją łańcuchową, złożoną z fotochemicznego wzbudzenia cząsteczki Cl2, która po absorpcji fotonu dysocjuje (rozpada się) na dwa bardzo aktywne atomy chloru, które reagują z cząsteczką wodoru, dając cząsteczkę produktu (HCl) i aktywny atom wodoru, ten z kolei w reakcji z cząsteczką chloru tworzy cząsteczkę chlorowodoru i atom chloru itd. Rzeczywisty przebieg reakcji chemicznej jest zwany mechanizmem reakcji.
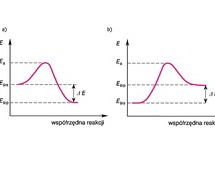
Reakcje biegną z szybkością określoną zmianą stężenia reagentów; szybkość tę można opisać empirycznym wzorem: v = k · cAα · cBβ, gdzie c — stężenia substratów, k — współczynnik proporcjonalności, niezmienny dla określonej reakcji w danej temperaturze, zwany stałą szybkości reakcji (równy szybkości reakcji, gdy stężenia reagentów są jednostkowe). Niektóre reakcje zachodzą bardzo szybko, np. rozkład materiału wybuchowego, reakcje fotochemiczne w gazach, inne to procesy bardzo wolne, np. przemiany chemiczne zachodzące w skorupie ziemskiej w czasie tysięcy lat. Jednym z parametrów wpływających na szybkość reakcji chemicznej jest temperatura — reguła van’t Hoffa podaje orientacyjnie, że podwyższenie temperatury o 10°C powoduje 2–4-krotny wzrost szybkości reakcji (zmiana stałej szybkości k; reakcja zachodząca w temperaturze pokojowej z niezauważalną szybkością może przebiegać wybuchowo po ogrzaniu reagentów). Tę zależność można wyjaśnić na gruncie kinetycznej teorii materii. Aby zaszła reakcja cząsteczki muszą się „spotkać”. W fazie gazowej są to bardzo częste, o bardzo krótkim czasie kontaktu zderzenia cząsteczek, które teoria ta rozpatruje jako kulki. Ogromna większość to zderzenia sprężyste, w których cząsteczki jedynie wymieniają energię i pęd. Do zderzeń efektywnych, tzn. prowadzących do utworzenia produktów, należą tylko te, w których biorą udział cząsteczki mające (w wyniku wielokrotnych zderzeń) odpowiednio wysoką energię — tzw. energię aktywacji (jej wartość jest charakterystyczna dla danej reakcji chemicznej). W wyniku podwyższania temperatury (tzn. dostarczania układowi energii) coraz większa liczba cząsteczek osiąga tę wartość. W roztworach cząstki nie są tak ruchliwe jak w gazach (liczba zderzeń jest dużo mniejsza), a mimo to reakcje przebiegają z podobną szybkością. Jest to spowodowane tzw. efektem klatkowania: uwięzienia kontaktujących się indywiduów w „klatce” utworzonej przez cząsteczki rozpuszczalnika, w wyniku czego czas kontaktu jest dużo dłuższy (20–100 razy) niż w przypadku fazy gazowej. Zderzenie cząsteczek obdarzonych energią równą energii aktywacji (lub jej bliską) prowadzi do utworzenia tzw. kompleksu aktywnego — nietrwałego układu, który może rozpaść się na cząsteczki substratów lub w wyniku oddziaływań elektronowych wytworzyć nowe wiązania chemiczne, tj. utworzyć cząsteczkę produktu. Jeśli średnia energia cząsteczkowa produktów jest mniejsza od średniej energii cząsteczek substratów, to reakcję chemiczną nazywa się reakcją egzoenergetyczną (lub egzoergiczną), w przypadku odwrotnym, gdy układowi trzeba dostarczyć energii ΔE — reakcją endoenergetyczną (endoergiczną). Gdy układ wymienia z otoczeniem energię w postaci ciepła mówi się odpowiednio o reakcji egzo- i endotermicznej. Reakcje chemiczne są w zasadzie odwracalne i biegną samorzutnie aż do osiągnięcia stanu równowagi chemicznej. W stanie równowagi szybkość tworzenia się produktów jest równa szybkości ich rozpadu na substraty — w danych warunkach (ciśnienia, temperatury, stężenia) współistnieją ze sobą wszystkie reagenty (co zapisuje się: αA + βB ⇌ γAB), a stosunek iloczynu stężeń produktów do iloczynu stężeń substratów reakcji jest wielkością stałą, charakterystyczną dla danej reakcji — tzw. stałą równowagi chemicznej: 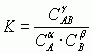 . Reakcje, których stan równowagi jest silnie przesunięty w stronę produktów, nazywa się nieodwracalnymi. Badaniem szybkości reakcji chemicznych zajmuje się kinetyka chemiczna. Do badania szybkości reakcji chemicznych, w których ustala się stan równowagi dynamicznej wykorzystuje się zwłaszcza metodę wskaźników izotopowych; do badania reakcji bardzo szybkich (np. przebiegających w czasie kilku pikosekund) stosuje się specjalne techniki, m.in. fotolizę błyskową, metody relaksacyjne. Kinetyką elementarnych etapów reakcji chemicznych zajmuje się femtochemia.
. Reakcje, których stan równowagi jest silnie przesunięty w stronę produktów, nazywa się nieodwracalnymi. Badaniem szybkości reakcji chemicznych zajmuje się kinetyka chemiczna. Do badania szybkości reakcji chemicznych, w których ustala się stan równowagi dynamicznej wykorzystuje się zwłaszcza metodę wskaźników izotopowych; do badania reakcji bardzo szybkich (np. przebiegających w czasie kilku pikosekund) stosuje się specjalne techniki, m.in. fotolizę błyskową, metody relaksacyjne. Kinetyką elementarnych etapów reakcji chemicznych zajmuje się femtochemia.
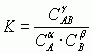 . Reakcje, których stan równowagi jest silnie przesunięty w stronę produktów, nazywa się nieodwracalnymi. Badaniem szybkości reakcji chemicznych zajmuje się kinetyka chemiczna. Do badania szybkości reakcji chemicznych, w których ustala się stan równowagi dynamicznej wykorzystuje się zwłaszcza metodę wskaźników izotopowych; do badania reakcji bardzo szybkich (np. przebiegających w czasie kilku pikosekund) stosuje się specjalne techniki, m.in. fotolizę błyskową, metody relaksacyjne. Kinetyką elementarnych etapów reakcji chemicznych zajmuje się femtochemia.
. Reakcje, których stan równowagi jest silnie przesunięty w stronę produktów, nazywa się nieodwracalnymi. Badaniem szybkości reakcji chemicznych zajmuje się kinetyka chemiczna. Do badania szybkości reakcji chemicznych, w których ustala się stan równowagi dynamicznej wykorzystuje się zwłaszcza metodę wskaźników izotopowych; do badania reakcji bardzo szybkich (np. przebiegających w czasie kilku pikosekund) stosuje się specjalne techniki, m.in. fotolizę błyskową, metody relaksacyjne. Kinetyką elementarnych etapów reakcji chemicznych zajmuje się femtochemia. Szybkość reakcji chemicznej można zmienić np. zmieniając temperaturę lub — głównie w przypadku reakcji prowadzonych w fazie gazowej — ciśnienia reagującego układu, wprowadzając katalizator (zmniejszający energię aktywacji), a także — zwłaszcza w przypadku reakcji heterogenicznych — zwiększając powierzchnię kontaktu reagujących substancji (rozdrabnianie, mieszanie, prowadzenie procesu przeciwprądowo, stosując fluidyzację).
Reakcje chemiczne dzieli się ogólnie na: reakcje syntezy (tworzenia): A + B = AB; reakcje analizy (rozkładu): AB = A + B; reakcje wymiany: AB + C = AC + B (wymiana pojedyncza, zwana podstawianiem) i AB + CD = AC + BD (wymiana podwójna). Zależnie od reagujących cząstek, mechanizmu, sposobu inicjowania rozróżnia się reakcje rodnikowe, jonowe, atomowe, cząsteczkowe oraz reakcje łańcuchowe, katalityczne, fotochemiczne, elektrodowe i in.