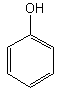
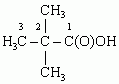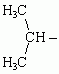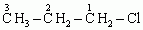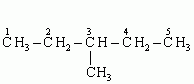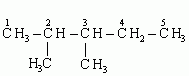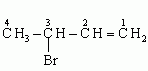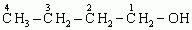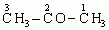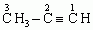Związki organiczne są substancjami gazowymi, ciekłymi lub stałymi, palącymi się lub podtrzymującymi palenie, rozkładającymi się na pierwiastki lub proste związki nieorganiczne (woda, tlenki węgla, chlorowodór) po podgrzaniu do temperatury ponad 1000°C bez dostępu tlenu. Budową, właściwościami, syntezą i przemianami związków organicznych zajmuje się chemia organiczna. Nazwa „związki organiczne” wywodzi się z czasów, kiedy uważano, że ich synteza może dokonywać się wyłącznie w organizmach żywych. W cząsteczkach związków organicznych występują wiązania kowalencyjne pojedyncze, podwójne, potrójne; szczególnie silne są wiązania między atomami węgla, charakterystyczne dla węgla pierwiastkowego; wiązania jonowe lub koordynacyjne występują w związkach organicznych znacznie rzadziej. Szacuje się, że liczba opisanych dotąd związków organicznych przekroczyła już 10 mln i rocznie zwiększa się o ok. 200 tysięcy. Ta mnogość związków organicznych wynika ze zdolności atomów węgla do tworzenia wiązań zarówno między własnymi atomami, jak i z atomami większości innych pierwiastków chemicznych; prowadzi to do powstawania cząsteczek o dowolnie dużej liczbie atomów, powiązanych ze sobą w łańcuchy i/lub pierścienie, różniące się między sobą (w przypadku takiego samego składu ilościowego i jakościowego) dodatkowo kolejnością wiązań oraz geometrycznym i/lub przestrzennym ułożeniem atomów w cząsteczce (izomeria). Związki organiczne dzieli się zależnie od budowy podstawowego szkieletu cząsteczki na: 1) organiczne związki acykliczne (łańcuchowe), w których łańcuch atomów węgla może zawierać różne kombinacje wiązań pojedynczych (związki nasycone) lub podwójnych i potrójnych (związki nienasycone); 2)
związki cykliczne (pierścieniowe), których łańcuchy tworzą jeden lub więcej pierścieni; pierścienie mogą być zbudowane tylko z atomów węgla (karbocykliczne związki) lub zawierać też heteroatomy (
związki heterocykliczne); związki karbocykliczne mogą być
związkami aromatycznymi, zawierającymi formalnie zamknięty, sprzężony układ wiązań podwójnych, lub
związkami alicyklicznymi, których pierścienie nie mają charakteru związków aromatycznych. Wśród związków organicznych występują także różne kombinacje wymienionych podstawowych grup związków. Związki organiczne dzieli się poza tym, zależnie od obecnych w ich cząsteczkach
grup funkcyjnych, na odpowiednie klasy (m.in.: związki fluorowcoorganiczne, alkohole, fenole, aldehydy, ketony, kwasy karboksylowe, kwasy sulfonowe, aminy, etery, związki nitrowe, związki krzemoorganiczne, fosforoorganiczne).
Nazewnictwo związków organicznych początkowo było tworzone w sposób niesystematyczny, często na podstawie pochodzenia danego związku (np. kwas winowy, mrówkowy, kofeina), albo wywodziło się od nazwiska odkrywcy (np. keton Michlera) lub charakterystycznych właściwości (oranż metylowy); nazwy niesystematyczne (zwyczajowe, trywialne) są używane do dziś (a czasem nawet tworzone dla związków o nie w pełni wyjaśnionej budowie), ale podstawowe znaczenie mają nazwy systematyczne, budowane według reguł określonych przez Międzynarodową Unię Chemii Czystej i Stosowanej (IUPAC) i oparte ściśle na strukturze związków organicznych; np. kwas piwalonowy (nazwa zwyczajowa), kwas trimetylooctowy (nazwa półsystematyczna), kwas 2,2-dimetylopropanowy (nazwa systematyczna) dla związku:
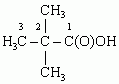
Nazwy systematyczne tworzy się z: 1) nazwy szkieletu podstawowego cząsteczki (decydującego o rdzeniu nazwy) z podaniem numeracji atomów w tym szkielecie; 2) nazwy dominującej grupy funkcyjnej (decydującej o końcówce nazwy) według określonej kolejności i z zaznaczeniem liczby tych grup; 3) nazwy podstawników (decydujących o przedrostku nazwy), czyli grup funkcyjnych niedominujących, rozgałęzień łańcucha lub dodatkowych pierścieni, z określeniem ich pozycji. Za szkielet podstawowy cząsteczki przyjmuje się najdłuższy prosty łańcuch atomów węgla lub wybrany układ pierścieniowy (np. zawierający największą liczbę grup dominujących lub największą liczbę wiązań wielokrotnych). Podstawą słownictwa systematycznego i półsystematycznego związków organicznych są nazwy węglowodorów nasyconych (alkanów lub cykloalkanów), prostych węglowodorów aromatycznych i związków heterocyklicznych, nazwy prostych grup organicznych — alkilów i arylów, oraz nazwy grup funkcyjnych; np. pierwsze człony szeregu węglowodorów nasyconych (alkanów) w kolejności według liczby atomów węgla mają następujące nazwy: metan, etan, propan, butan, pentan, heksan, heptan, oktan itd.; nazwy grup organicznych tworzy się przez zmianę końcówki nazwy węglowodorów, np.:
CH3–
metyl (od metanu)
CH3CH2–
etyl (od etanu)
CH3–CH=CH–
1-propenyl (od propenu)
–CH2–(CH2)3–CH2–
pentametylen (od pentanu)
izopropyl (od izopropanu)
CH2=CH–
etenyl, potocznie winyl (od etenu)
CH≡C–
etynyl (od etynu)
Przykłady nazw prostych związków organicznych:
1-chloropropan lub chlorek propylu
CH3–O–CH3
eter dimetylowy lub metoksymetan
3-metylopentan
2,3-dimetylopentan
3-bromobut-1-en
butan-1-ol lub alkohol butylowy
propanon lub aceton
propyn lub metyloacetylen
hydroksybenzen lub fenol
Bardzo wiele związków organicznych występuje w przyrodzie (składniki ropy naftowej, gazu ziemnego, węgli kopalnych); związki organiczne stanowią, oprócz wody, główny składnik wszystkich organizmów żywych. W przeszłości głównym źródłem związków organicznych były surowce naturalne; obecnie wytwarza się je syntetycznie. Związki organiczne są szeroko stosowane w życiu codziennym i w praktyce przemysłowej jako paliwa, tworzywa sztuczne, włókna syntetyczne, barwniki, lekarstwa, środki powierzchniowo czynne, środki ochrony roślin, materiały wybuchowe, środki zapachowe i kosmetyczne, a także jako półprodukty do ich wytwarzania.