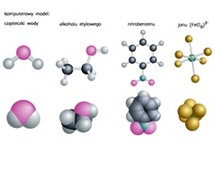
woda, tlenek diwodoru, oksydan, H2O,
związek tlenu i wodoru;
woda
Encyklopedia PWN
bezbarwna ciecz, w grubych warstwach, zielononiebieska, bez smaku i zapachu; temperatura krzepnięcia 0°C, temperatura wrzenia 100°C; występuje w 3 stanach skupienia: stałym (lód), ciekłym i gazowym (para wodna), które współistnieją tylko w temperaturze 0,01°C przy ciśnieniu 611,73 Pa. Polaryzacja wiązań w cząsteczce wody (nadmiar ładunku ujemnego na atomie O i dodatniego na atomach H) powoduje, że wykazuje ona elektryczny moment dipolowy 6,1 · 10–30 C · m (1,83 D). Polarne cząsteczki H2O w lodzie łączą się oddziaływaniami elektrostatycznymi, tworząc między sobą wiązania wodorowe w taki sposób, że upakowanie cząsteczek jest mniej zwięzłe niż w wodzie ciekłej, co powoduje anomalię, polegającą na tym, że lód ma gęstość mniejszą niż woda ciekła. W czasie topnienia w 0°C tylko część wiązań wodorowych zostaje zerwana i w cieczy pozostają ugrupowania cząsteczek; ze wzrostem temperatury ulegają one dalszemu rozpadowi i gęstość cieczy w anormalny sposób rośnie ze wzrostem temperatury, by w temperaturze 3,98°C osiągnąć wartość maksymalną 0,99995 g/cm3; dalsze ogrzewanie powoduje zmniejszanie gęstości normalnie obserwowane u wszystkich cieczy. Obecność wiązań wodorowych jest przyczyną anormalnie wysokiej temperatury topnienia i temperatury wrzenia wody, a także innych parametrów fizycznych (m.in. względnej przenikalności elektrycznej, ciepła właściwego). Wartości temperatury: topnienia, wrzenia, punktu potrójnego wody służą jako wzorcowe punkty stałe przy wyznaczaniu skal temperatury. Woda w nieznacznym stopniu ulega dysocjacji elektrolitycznej (autojonizacji): H2O ⇌ H+ + OH− (jon H+ występuje jako jon oksoniowy H3O+). W czystej wodzie stężenia jonów H+ i OH− są jednakowe — woda wykazuje odczyn obojętny (pH = 7,0). Woda jest dobrym rozpuszczalnikiem wielu substancji (zwłaszcza polarnych), także katalizatorem wielu reakcji chemicznych. Tlenki metali reagując z wodą tworzą zasady, tlenki niemetali — kwasy, niektóre metale łączą się z nią (szczególnie energicznie litowce) z wydzieleniem wodoru i powstaniem wodorotlenków.
Woda jest trwałym związkiem chemicznym najbardziej rozpowszechnionym w przyrodzie (hydrosfera) i znajduje się w stałym obiegu; występuje też w stanie związanym jako woda konstytucyjna, krystalizacyjna i zeolityczna; stanowi jeden z podstawowych składników wszystkich żywych organizmów, umożliwiający przemianę materii i biorący udział w wielu jej procesach; żywa komórka zawiera 75–85% wody; w środowisku wodnym powstało życie; dla licznych zwierząt i roślin stanowi ona jedyne środowisko życia. Dla świata istot żywych bardzo ważne są: duża wartość ciepła właściwego i ciepła krzepnięcia wody oraz specyficzna zależność gęstości od temperatury. Te cechy wody sprawiają, że wahania temperatury w środowisku wodnym są mniejsze niż na lądzie — duże zbiorniki wodne wolno się nagrzewają i ochładzają, łagodząc także klimat przyległych lądów. Zwiększanie się gęstości wody wywołane jej ochładzaniem jest przyczyną opadania chłodniejszych warstw na dno zbiornika i wypływania na powierzchnię warstw cieplejszych, lżejszych. Dalsze ochładzanie powoduje powstanie lodu na powierzchni i zaleganie warstw wody (o temperaturze ok. 4°C) w głębi zbiornika — pozostają one nie zamarznięte i może się w nich toczyć aktywne życie. Wody naturalne (np. morskie, mineralne) zawierają zwykle rozpuszczone sole i gazy, a także bakterie i in. drobnoustroje oraz zawiesiny substancji nieorganicznych; woda zawierającą duże ilości soli wapnia i magnezu nazywa się wodą twardą. Woda ma szerokie zastosowanie; jest używana do spożycia, do celów gospodarczych, w przemyśle; jest niezbędna do przebiegu wielu procesów technologicznych (jako rozpuszczalnik, substrat lub katalizator reakcji chemicznych); stosowana do rozdzielania (np. flotacja) i oczyszczania substancji (np. krystalizacja); wykorzystywana jako nośnik ciepła (chłodzenie, ogrzewanie); energię mechaniczną wód naturalnych przetwarza się na inne rodzaje energii; parę wodną wykorzystuje się do poruszania turbin parowych i parowych silników tłokowych.