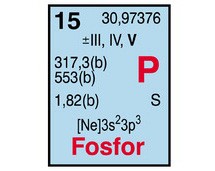
fosfor, P, phosphorus,
pierwiastek chemiczny o liczbie atomowej 15;
Symbol: P
Nazwa łacińska: Phosphorus
Liczba atomowa: 15
Pierwiastek promieniotwórczy: nie
Grupa układu okresowego pierwiastków: 15 — azotowce
Odkrycie: 1669
Odkrywca: Brand Hennig