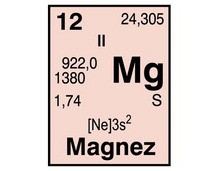
magnez, Mg, magnesium,
pierwiastek chemiczny o liczbie atomowej 12;
Symbol: Mg
Nazwa łacińska: Magnesium
Liczba atomowa: 12
Pierwiastek promieniotwórczy: nie
Grupa układu okresowego pierwiastków: 2 — berylowce
Odkrycie: 1829; (1808 – H.B. Davy)
Odkrywca: Bussy Antoine Alexandre Brutus, Liebig Justus